AI药物研发平台在《自然-通讯》发布最新研究成果
全球健康药物研发中心(GHDDI)与微软研究院科学智能中心合作开发了AI药物设计平台TamGen,并于10月29日在《自然-通讯》(Nature Communications)上发布了最新研究成果。TamGen通过基于Transformer自注意力机制的生成式AI模型,实现了针对致病靶蛋白的分子精准生成、优化以及合成与生物实验验证,开辟了创新药物发现的新路径,特别是在抗药性结核病等传染性疾病的研究中有广阔应用前景。

目前,该平台设计的分子在活性化合物实验筛选中取得了良好效果,研究人员成功发现设计出14种对结核杆菌ClpP蛋白酶表现出显著抑制活性的化合物。其中,最有效的化合物显示出半数最大抑制浓度(IC50)为1.9μM。
生成式药物设计面临的挑战
以ChatGPT为代表的生成式AI技术正在彻底改变药物研发领域。生成式药物设计能够从零开始创建全新分子或化合物,而无需依赖于现有的模板或分子框架。传统筛选方法,如高通量筛选、虚拟筛选,以及最新的基于深度学习的筛选,通常从包含10,000到1亿个分子的化合物库中寻找候选药物。而生成式药物设计则可以探索广阔的化学空间,估计这个空间包含超过10的60次方个潜在化合物。
这种方法有望发现一些未被充分研究的化合物类别,以及不在现有库中的新型化合物。然而,以往生成式方法生成的化合物往往缺乏令人满意的药物特性。这些方法通常只关注有限的药物相关属性,未能显著提高后续药物发现过程的成功率。另外,即使采用多种虚拟筛选技术,在如此庞大的化学空间中针对不同靶点进行筛选仍需要大量计算资源和时间,同时需考虑模型准确率的影响。换句话说,尽管AI生成了大量新型化合物,但现有方法在提供有效候选药物方面仍然面临挑战。
TamGen让AI有的放矢
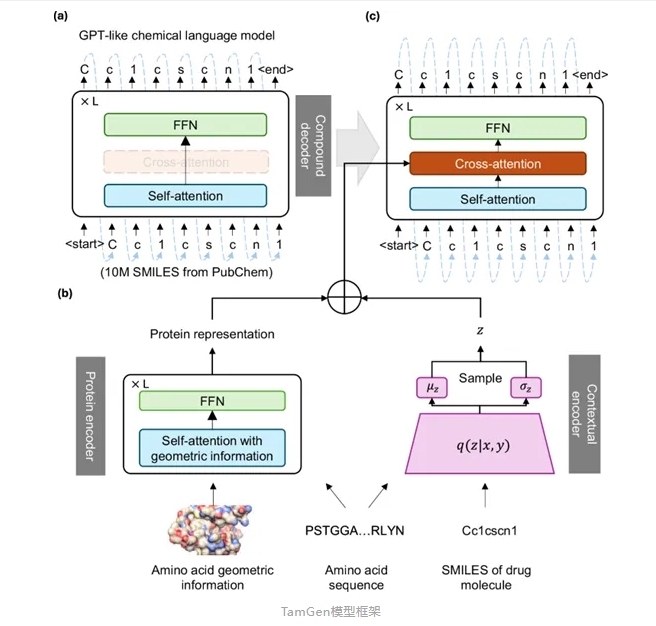
为了应对生成式药物设计面临的挑战,全球健康药物研发中心(GHDDI)与微软研究院科学智能中心联合开发了TamGen。其创新之处在于,在类GPT生成模型的基础上加入了交叉注意力机制,并通过学习大量的已知和模拟的蛋白-配体结构数据,使得模型在生成新的化学分子时,能够同时考虑致病靶蛋白的信息。这一改进使TamGen能够基于靶蛋白活性位点信息精准生成具备潜在相互作用的分子,进而增强分子生成的靶向性以及药物设计的合理性与精准度,再结合分子模拟、细胞活性AI模型与专家经验进一步虚拟筛选与优化,从而大幅提升发现候选药物的效率与成功率。GHDDI数据科学平台负责人郭博士表示:“传统的生成式AI设计方法更像是先造出无数把钥匙,再一把一把地试能否打开门。而TamGen则像是在比对锁眼,更精确地匹配钥匙。”
未来展望
下一步,TamGen的工作方向将集中在整合更多三维生成方法的优势,比如采用蒙特卡洛树搜索(Monte Carlo Tree Search,MCTS)或分子动力学模拟技术,进一步改善生成化合物与靶蛋白结合能力及其他重要药物性质,如稳定性、合成可能性以及ADME/T特性。
GHDDI中心主任丁胜表示:“TamGen的初步成果标志着生成式药物设计领域的一项重要创新,为未来的AI药物研发提供了强有力的实用性和适用性证据。随着人工智能技术在药物发现领域的持续进步,TamGen有望加速新药研发,帮助应对包括结核病在内的多种公共卫生挑战。”


